
|
О НАНОМЕХАНИКЕ ТЕМНОЙ И СВЕТЛОЙ МАТЕРИИ
Михаил Яковлевич Иванов, д.ф.-м.н
"Нашей души родовые зачатки
во много раз меньше
Нежели те, из которых слагаются тело с утробой".
Тит Лукреций Кар "О природе вещей".
(Окончание. Начало в № 5 - 2008)
Водородная и ионная связи
В рамках модели СТационарных ЭЛектронов
(СТЭЛ) естественным образом представляется модель водородных связей,
когда на первой, ближайшей к протону (иону водорода) оболочке, стационарно
локализуются два электрона, одновременно принадлежащих двум другим ионам.
Например, отрицательный ион дифторида водорода HFa-, обладающий линейной
структурой F-H-F-, обязан своей устойчивостью протону, который путем
кулоновского взаимодействия связывает два отдельных иона фтора. Отметим,
что водородные связи играют важную роль в удержании двух цепей спиралевидной
структуры молекулы ДНК.
Ионная связь представляет собой кулоновское взаимодействие, при этом
внешние электроны одного атома дополняют более заполненную внешнюю оболочку
другого атома. Здесь также удобно для элементов второго и третьего периода
таблицы Менделеева рассматривать октеты стационарных электронов внешних
оболочек с геометрическим представлением в форме антипризм. Характерными
примерами служат хлористый натрий и сернистый магний.
Полярные и неполярные молекулы
Распределение положительных и отрицательных зарядов определяет наличие или отсутствие у молекулы электрического дипольного момента. Величина дипольного момента молекулы задает ряд важных свойств вещества и находится экспериментальным путем. Предложенный нами метод СТЭЛ позволяет теоретически наглядно объяснить и рассчитать величину дипольного момента различных молекул.
Из рассмотрения проиллюстрированной структуры молекул кислорода O2, азота N2, диоксида углерода CO2, а также сероуглерода CS2 и диоксида кремния SiO2 сразу же следует, что эти молекулы являются неполярными и их дипольный момент равен нулю. В то же время молекулы воды H2O, окиси углерода CO, сероводорода H2S и диоксида серы (сернистого ангидрида) SO2 являются полярными и имеют отличный от нуля дипольный момент. Рассчитанный теоретически на основе метода СТЭЛ дипольный момент приведенных ранее примеров молекул хорошо согласуется с имеющимися экспериментальными данными. Данное обстоятельство представляет собой веское экспериментальное доказательство справедливости метода СТЭЛ.
Примеры сложных молекул
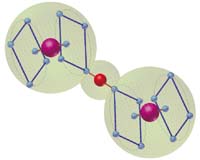 В
качестве примеров приведем структуры аллотропных модификаций углерода.
Первый пример демонстрирует "одномерную" кристаллическую модификацию
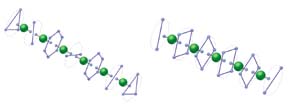
углерода с цепочным строением молекул, называемую карбин. Цепи карбина
имеют либо поликумуленовое (= C = C =), либо полиеновое (-C ≡
C-) строение. Отсюда получаем соответствующие элементы цепочного строения
на основе метода СТЭЛ.
В
качестве примеров приведем структуры аллотропных модификаций углерода.
Первый пример демонстрирует "одномерную" кристаллическую модификацию
углерода с цепочным строением молекул, называемую карбин. Цепи карбина
имеют либо поликумуленовое (= C = C =), либо полиеновое (-C ≡
C-) строение. Отсюда получаем соответствующие элементы цепочного строения
на основе метода СТЭЛ.
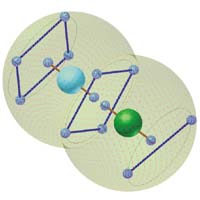
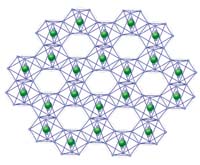
Следующий пример относится к "двумерным" кристаллическим модификациям углерода - графиту в двух его формах. Первая форма - графен с двумерной кристаллической решеткой типа "пчелиных сот". Каждый атом углерода на плоскости соединен с тремя соседними атомами обычной ковалентной связью. Слои графена при многослойной реализации соединены более слабыми связями. В случае пиролитического графита атомы углерода соединены ионными связями.
О возможном механизме биомолекулярной памяти
Современные компьютерные технологии на полупроводниковых кристаллах (кремниевых чипах) имеют принципиальные ограничения по плотности хранения информации. Эти ограничения обусловлены собственной кристаллической структурой чипов и природой элемента информации (бита), когда роль носителя информации исполняет электрон - дырочная пара. В качестве предельного минимального размера для хранения бита информации здесь можно принять размер атома кремния, а минимальный электрический заряд, переносимый в процессе запоминания бита информации, - заряд электрона.
 Реализованная
природой плотность хранения биологической информации превышает все мыслимые
пределы. Так, одна молекула дезоксирибонуклеиновой кислоты (молекула
ДНК) содержит всю генетическую информацию о будущих поколениях организма.
В этом случае надо допустить наличие существенно более высокой (на многие
порядки величины) плотности хранения информации, чем в предельном случае
кремниевых технологий. В то же время, несмотря на активные исследования
в области биокомпьютеров, в течение последних 15 лет механизм записи
и хранения информации в молекулах ДНК остается загадкой. Далее представляем
описание механизма биомолекулярной памяти на основе ТМ, когда роль носителя
информации (бита) будет исполнять элементарная частица (диполь) ТМ,
роль чипа - молекула ДНК.
Реализованная
природой плотность хранения биологической информации превышает все мыслимые
пределы. Так, одна молекула дезоксирибонуклеиновой кислоты (молекула
ДНК) содержит всю генетическую информацию о будущих поколениях организма.
В этом случае надо допустить наличие существенно более высокой (на многие
порядки величины) плотности хранения информации, чем в предельном случае
кремниевых технологий. В то же время, несмотря на активные исследования
в области биокомпьютеров, в течение последних 15 лет механизм записи
и хранения информации в молекулах ДНК остается загадкой. Далее представляем
описание механизма биомолекулярной памяти на основе ТМ, когда роль носителя
информации (бита) будет исполнять элементарная частица (диполь) ТМ,
роль чипа - молекула ДНК.
 Прежде
всего укажем, что в нашем случае молекула ДНК имеет реально существующие
в стационарном фиксированном состоянии электроны и атомы, погруженные
в реально существующее пространство ТМ (здесь мы полностью отказываемся
от квантовомеханических представлений). Напомним, что молекула ДНК представляет
собой биополимер, мономером которого является нуклеотид. Нуклеотиды
соединены между собой ковалентно в длинные полинуклеотидные цепи. Эти
цепи, в свою очередь, попарно соединены водородными связями в закрученную
структуру, получившую название двойной спирали. Поперечный размер двойной
спирали составляет от 22 до 24 ангстрем или 2,2...2,4 нм, длина каждого
нуклеотида - 0,33 нм. Подобно тому, как на винтовой лестнице сбоку видны
ступеньки, на двойной спирали ДНК в промежутках между фосфатными остовами
молекул можно видеть ребра азотистых оснований нуклеотидов.
Прежде
всего укажем, что в нашем случае молекула ДНК имеет реально существующие
в стационарном фиксированном состоянии электроны и атомы, погруженные
в реально существующее пространство ТМ (здесь мы полностью отказываемся
от квантовомеханических представлений). Напомним, что молекула ДНК представляет
собой биополимер, мономером которого является нуклеотид. Нуклеотиды
соединены между собой ковалентно в длинные полинуклеотидные цепи. Эти
цепи, в свою очередь, попарно соединены водородными связями в закрученную
структуру, получившую название двойной спирали. Поперечный размер двойной
спирали составляет от 22 до 24 ангстрем или 2,2...2,4 нм, длина каждого
нуклеотида - 0,33 нм. Подобно тому, как на винтовой лестнице сбоку видны
ступеньки, на двойной спирали ДНК в промежутках между фосфатными остовами
молекул можно видеть ребра азотистых оснований нуклеотидов.
 В
настоящее время считается, что только 1,5% генома человека состоит из
кодирующих блоков клеток, а более 50% ДНК человека состоит из некодирующих
повторяющихся последовательностей ДНК, что представляет собой неразрешенную
пока загадку природы. Далее мы не будем углубляться в особенности строения
молекулы ДНК, отправляя заинтересованного читателя к специальной литературе.
В
настоящее время считается, что только 1,5% генома человека состоит из
кодирующих блоков клеток, а более 50% ДНК человека состоит из некодирующих
повторяющихся последовательностей ДНК, что представляет собой неразрешенную
пока загадку природы. Далее мы не будем углубляться в особенности строения
молекулы ДНК, отправляя заинтересованного читателя к специальной литературе.
Остановимся на вопросе предельного минимального размера (бита) информации в случае молекулы ДНК. Если будем считать, что хранение бита биологической информации определяется наличием и размером одной водородной связи в молекуле ДНК, то в таком случае кремниевые чипы могли бы обеспечить более высокую плотность хранения информации. В связи с чем мы приходим к необходимости допустить возможность хранения бита биологической информации на другой, существенно более миниатюрной основе. Как предельно малый бит биологической информации здесь следует рассмотреть элементарную частицу (диполь) ТМ. В качестве биологического чипа огромной емкости естественно выступает спиралевидная молекула ДНК со своим поляризованным пространством ТМ. Генерируемые живым организмом слабые электромагнитные импульсы вполне достаточны, чтобы обеспечить запись и считывание информации в молекулах ДНК, которая имеет аналоговый (не цифровой) характер.
Подобным весьма качественным описанием вопроса записи и хранения биологической информации мы завершаем изложение наномеханических аспектов темной и светлой материи.
Автор выражает искреннюю признательность А.В. Малинину за плодотворные обсуждения и помощь в подготовке статьи.
[Напоминаем, что Интернет-вариант
статьи сильно сокращен. Ред.]